Обнаружение лекарств является трудоемким, дорогостоящим и часто склонным к неудачам, но разработка и моделирование лекарств с помощью компьютера может ускорить и улучшить разработку методов лечения. ,
Томас Читам – профессор медицинской химии и директор Центра высокопроизводительных вычислений в университете Юта и Родриго Галиндо, профессор в своей группе, используют мощные суперкомпьютеры для прогнозирования характеристик новых лекарств.
Недавно они использовали Frontera, самые быстрые суперкомпьютеры в любом университете в мире, и Longhorn, систему IBM / NVIDIA в Техасском центре передовых вычислений (TACC), для быстрого создания молекулярных моделей соединений, имеющих отношение к COVID. – 19, в сотрудничестве с химиками-медиками.
То, как молекулы изгибаются, связываются или реагируют с белками в клеточной среде, сильно зависит от их молекулярных силовых полей (не в звезде Поясните смысл термина, а скорее потенциальную энергию системы взаимодействующих атомов). Тем не менее, силовые поля чрезвычайно сложно точно прогнозировать.
Один из ведущих инструментов, используемых для моделирования силовых полей и их влияние на связывание – Amber (Assisted Model Building с уточнением энергии), набор молекулярного моделирования программного обеспечения и силовых полей, для которого Cheatham является одним из главных разработчиков. Известный как один из первых кодов сообщества, Amber также развивается с тех пор 1978; его симуляции и силовые поля становятся более точными с каждым годом.
Для сравнительно простых структур, янтарь может соответствовать экспериментальные результаты с точностью до половины ангстрема (Å) – ста миллионных долей сантиметра, 10 – 10 метр.
Читам и Галиндо применяют Янтарь для биомолекулярного моделирования с применением в медицине. «Цель состоит в том, чтобы понять структуру, функции, динамику и энергетику биомолекулярных систем в их естественной среде с водой и другими лигандами».
Они участвовали в двух биомолекулярных исследованиях – изучали многообещающий класс соединений меди, борющихся с раком, и выясняли, как экспериментальные модификации основной цепи ДНК могут противостоять деградации в организме – когда COVID – 19 пандемия поражена.
Читам и Галиндо быстро обратили свое внимание на поиск лекарств, способных разрушить коронавирус.
В 2015 при поддержке гранта NSF RAPID Cheatham разработал подход для быстрой идентификации молекулы, чтобы остановить вирус Эбола. Рабочий процесс, основанный на известных кристаллических структурах, использует программный пакет Rosetta для выбора многообещающих боковых цепей аминокислот на матрице с фиксированным пептидным скелетом, а затем выполняет молекулярно-динамическое моделирование с помощью Amber для оптимизации структур, которые затем ранжируются на основе оценок свободной энергетики.
Галиндо быстро сгенерировал более 2, 000 молекулярные модели соединений, релевантных для COVID – 19 используя этот подход на суперкомпьютерах Longhorn и Frontera в TACC. Успех этих усилий побудил Cheatham и Galindo подать заявку и получить 2,7 миллиона узловых часов в Blue Waters, еще одной системе на базе графического процессора, расположенной в Национальном центре суперкомпьютерных приложений (NCSA), для продолжения своих усилий
Награда была предоставлена через COVID – 19 Консорциум HPC – государственно-частный консорциум, работающий над поиском исследователей ресурсов для ускорения исследований вирусов.
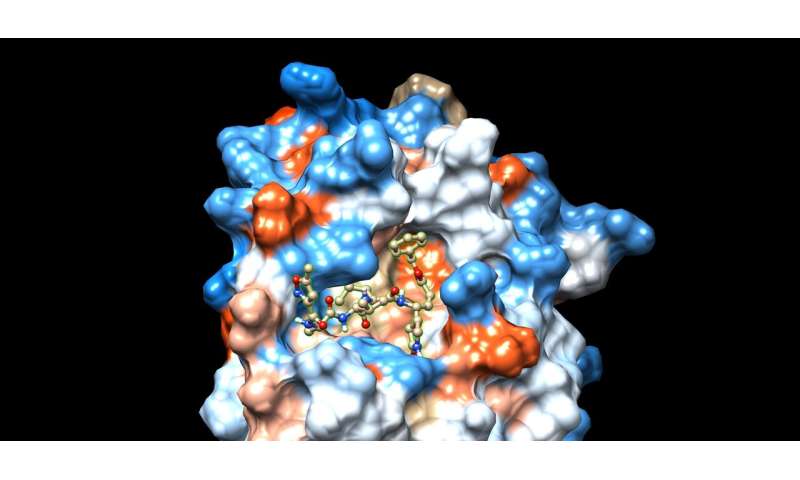
Они изучают кристаллическую структуру COVID – 19 main протеаза – фермент, который расщепляет белки и пептиды – в комплексе с пептидным ингибитором N3, который был недавно опубликован. Они планируют применить рабочий процесс разработки пептида Эбола к этой системе, чтобы изучить возможности COVID – 19 main Протеаза разрушает серию похожих, легко обнаруживаемых зондов, которые уже разработаны. Это послужит основой для анализа протеаз, которые проверяют эффективность ингибиторов.
Пептидные отведения будут позже будет преобразован в циклически модифицированные пептиды лабораторией Шмидта на кафедре медицинской химии в университете штата Юта, которая имеет значительный опыт в этой области. Циркулярные пептиды являются перспективными каркасами для биофармацевтических препаратов, которые можно применять для ингибирования межбелковых взаимодействий и ингибирования протеаз.
Читам и его команда были одними из первых, кто использовал системы Longhorn и Frontera для COVID – 19 исследование. Этот доступ помогает ускорить выбор вариантов лечения.
«Мы надеемся, что мы найдем новый пептид ингибитор, который может быть экспериментально проверен в ближайшие пару недель “, – сказал Читам. «И затем мы будем заниматься дальнейшим дизайном, чтобы сделать пептид циклическим, чтобы сделать его более стабильным в качестве потенциального лекарственного средства. Надеемся, что мы сможем в ближайшие несколько месяцев найти и экспериментально проверить лучший пептидный ингибитор для основной протеазы COVID». «.